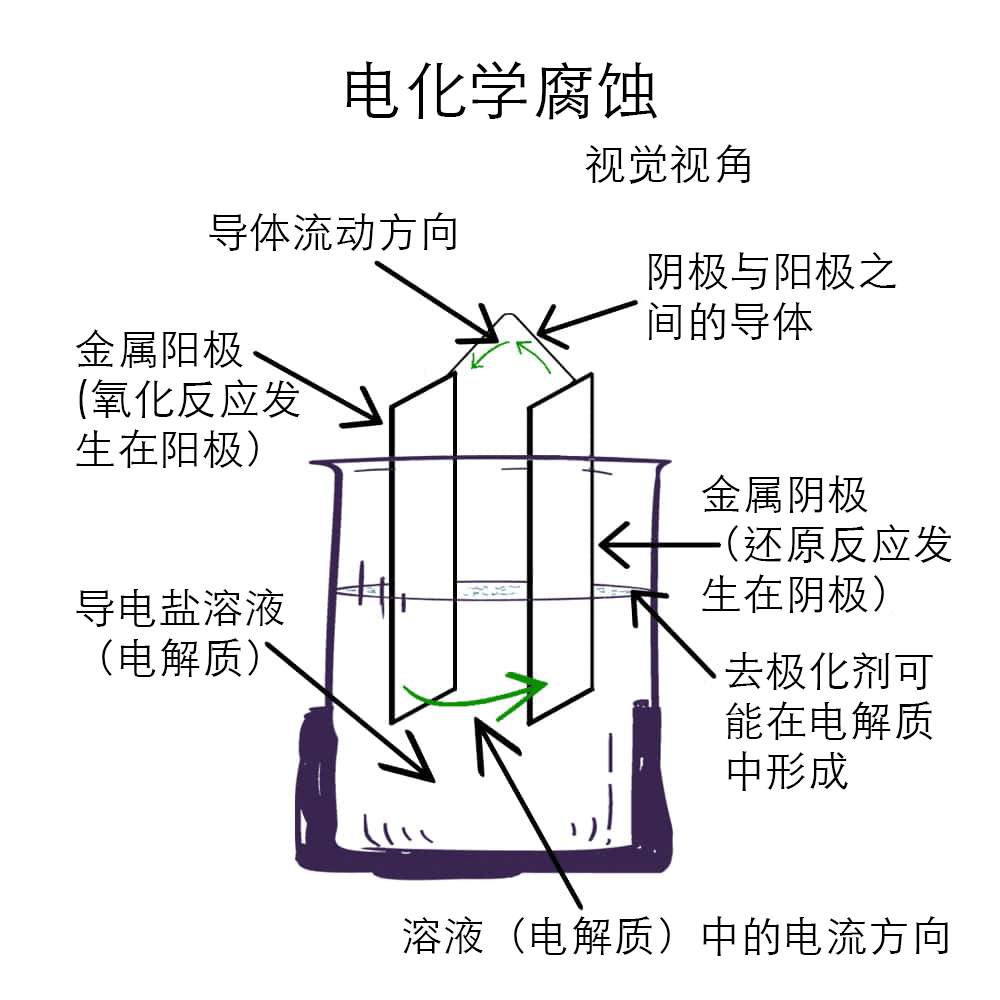
当两种不同金属在电解质(如水分或盐水)存在下发生电接触时,就会产生电化学腐蚀。此时阳极性更强的金属会加速腐蚀,而阴极性更强的金属则受到保护。以下是常见金属及其在电化学配对中的行为表现:
- 锌: 高度阳极性——接触不锈钢、铜或黄铜时会迅速腐蚀。
- 铝: 阳极性——当与铜或不锈钢等更贵金属配对时易受腐蚀。
- 碳钢/低合金钢: 中等活性——与青铜或不锈钢等阴极金属配对时可能发生腐蚀。
- 铜: 阴极——促进锌、铝或镀锌钢等较低贵金属的腐蚀。
- 黄铜与青铜: 阴极性——当直接接触时,常导致铝和钢的腐蚀。
- 不锈钢: 高度阴极性——加速邻近阳极金属(如锌或铝)的腐蚀。
电化学序列: 该电化学序列将金属从最阳极(活性)到最阴极(贵金属)进行排序。当两种金属在序列中相距越远,接触时发生电化学腐蚀的风险就越高。
预防提示:
- 分离异种金属: 使用垫圈、衬套或非导电隔离物来断开电气接触。
- 涂覆表面保护层: 使用保护性涂层来保护一种或两种金属免受电解质的侵蚀。
- 选择兼容材料: 选择在电化学序列中位置相近的金属,以最大限度地减少电位差。
了解不同金属之间的相互作用,有助于预防电化学腐蚀并延长设备使用寿命。